Présentation du projet
Qu’est ce que le dispositif Article 51 ?
La loi de financement de la sécurité sociale pour 2018 a introduit, en son article 51, un dispositif permettant d’expérimenter de nouvelles organisations en santé reposant sur des modes de financement inédits. Et ce, dès lors que ces nouvelles organisations contribuent à améliorer le parcours des patients, l’efficience du système de santé, l’accès aux soins ou encore la pertinence de la prescription des produits de santé.
Il s’agit là d’une véritable opportunité pour tester de nouvelles approches puisque ce dispositif permet de déroger à de nombreuses règles de financement de droit commun, applicables en ville comme en établissement hospitalier ou médico-social.
L’expérimentation Art 51 Onco’Link – Thérapies Orales est la plus grande expérimentation en cours et rassemble 45 sites expérimentateurs au travers tout le territoire.
Historique de l’expérimentation
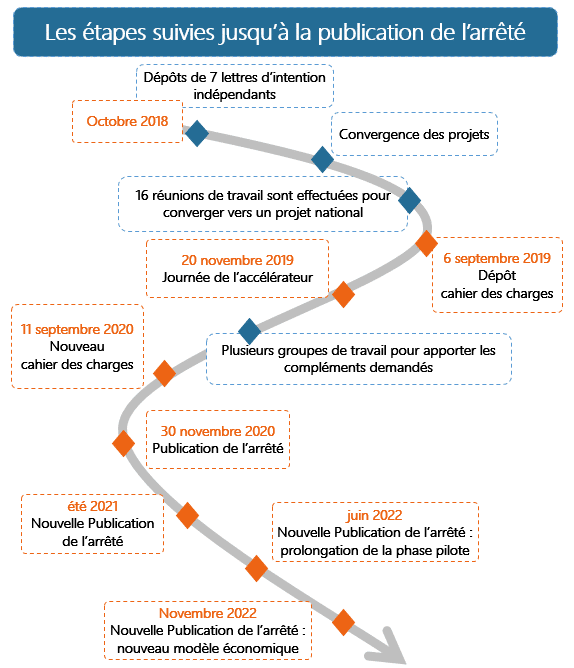
L’expérimentation Onco’Link Thérapies Orales a vu le jour à la suite du dépôt indépendant de 8 lettres d’intention, rassemblant 34 établissements hospitaliers, portant un parcours coordonné ville-hôpital pour accompagner la prise en charge des patients sous anticancéreux oraux.
Le ministère a pu prendre la mesure de l’importance de ce sujet tant pour les professionnels que pour la prise en charge des patients et a encouragé les établissements à mener en commun cette expérimentation à un niveau national.
Deux ans plus tard, le 9 décembre 2020, le cahier des charges est publié au JO et l’expérimentation rassemble 45 sites expérimentateurs sur tout le territoire.
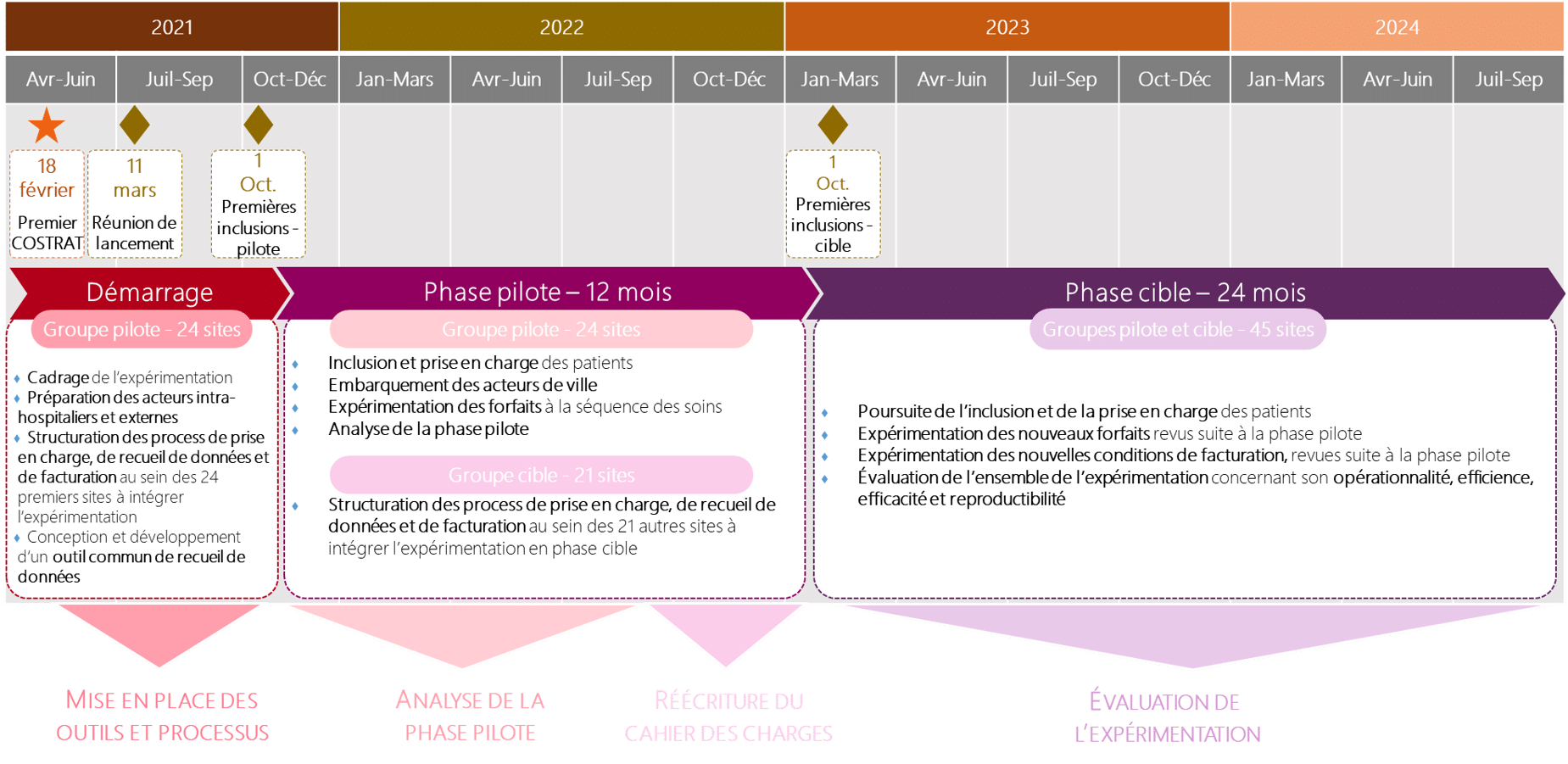
Au vu de l’ampleur exceptionnelle du projet, les discussions avec les instances de tutelles ont permis de concevoir cette expérimentation en 2 temps.
- Phase pilote, d’une durée de 12 mois, avec 24 sites expérimentateurs et 2 003 patients inclus
- Phase cible, d’une durée de 24 mois, avec 45 sites
Les inclusions de patients ont débuté le 1er octobre 2021.
A la fin de la phase pilote, un nouveau cahier des charges a été publié avec un nouveau modèle économique pour l’expérimentation.
Quels sont les objectifs d’Onco’Link –
Thérapies Orales ?
Les anticancéreux oraux sont des médicaments innovants représentant une dépense importante pour l’assurance maladie. La file active des patients sous thérapies orales dans les établissements hospitaliers ayant des services en cancérologie est de plus en plus importante, ce qui implique l’organisation d’une prise en charge hors les murs. A l’instar des chimiothérapies par voie intraveineuse, la gestion des effets indésirables et de l’observance sont des éléments clés dans le traitement du cancer. Cependant, force est de constater que les avantages de ce mode de prise médicamenteuse sont aussi à l’origine de potentiels dysfonctionnements qui influent sur l’efficacité du traitement.
L’expérimentation proposée a un double objectif stratégique :
- D’une part, l’amélioration de la qualité du suivi des patients sous thérapies orales à domicile
- D’autre part, la baisse de la consommation des soins liés aux complications et au mauvais suivi du traitement de ces patients.
Onco’Link – Thérapies Orales
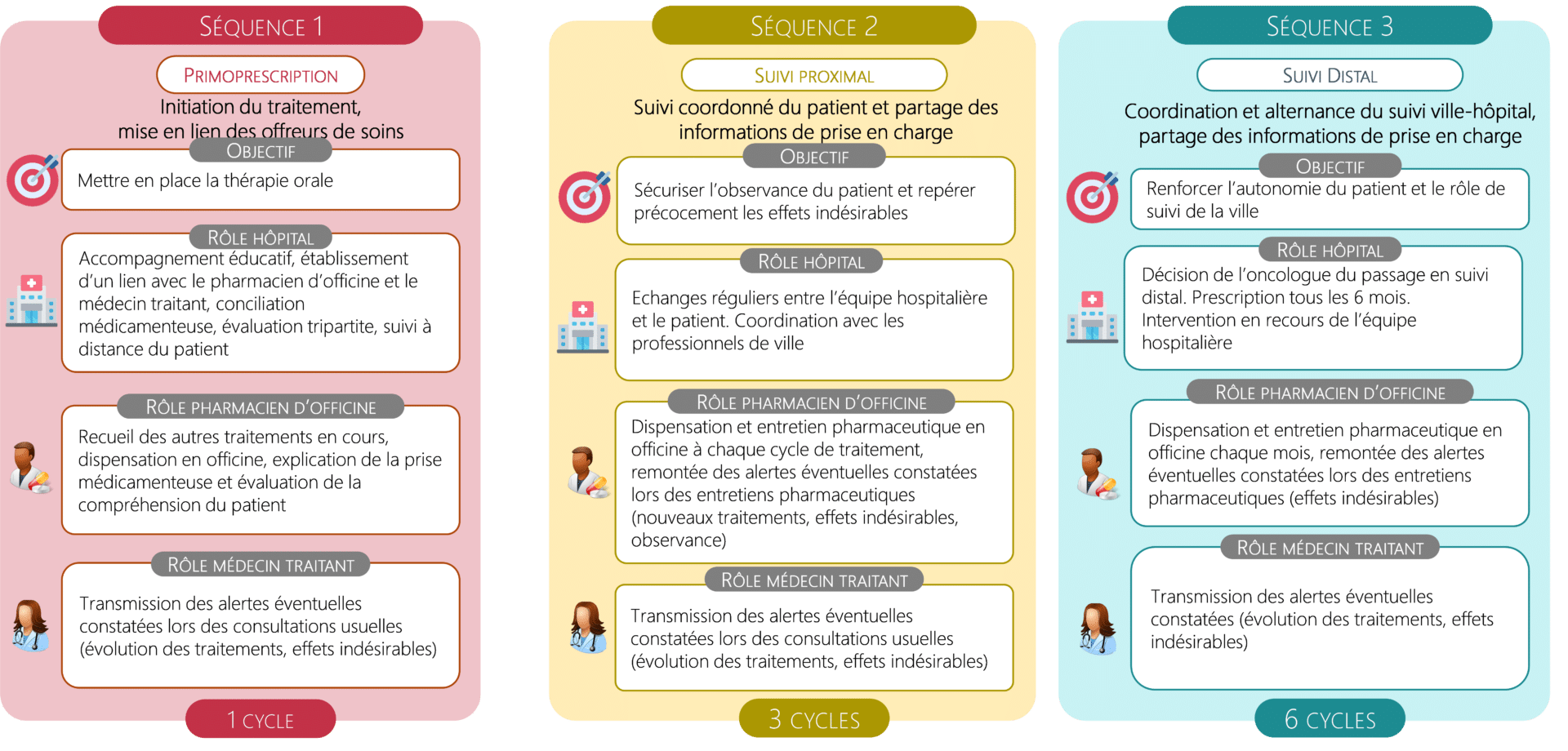
Un parcours patient organisé en 3 séquences
Une innovation organisationnelle
Un parcours innovant par la mise en place d’un circuit pluri professionnel ville-hôpital, appuyé par des échanges réguliers entre l’équipe hospitalière et le patient, un entretien pharmaceutique à chaque dispensation d’anticancéreux oraux, et une coordination entre les professionnels de ville et de l’hôpital.
Un nouveau mode de financement
Un mode de financement innovant construit par séquence de soins.
L’investissement de chaque acteur du parcours (établissement hospitalier, pharmacien et médecin traitant) est valorisé par une rémunération forfaitaire déclenchée en fin de chaque séquence.
Les patients concernés
Les critères d’inclusion dans l’expérimentation sont :
- Les patients majeurs atteints de cancers solides et hématologiques
- Les patients allant débuter un traitement anticancéreux oral (dont hormonothérapie en situation métastatique)
- Les patients dont le traitement anticancéreux sera pris à domicile (hors HAD)
- Les patients affiliés à un régime de la sécurité sociale ou bénéficiaires d’un tel régime
Les critères de non-inclusion dans l’expérimentation sont :
- Les patients mineurs (<18 ans)
- Hormonothérapie en situation adjuvante
- Les patients incapables de souscrire aux modalités de suivi prévues par le protocole de l’expérimentation de manière autonome selon l’avis du médecin référent
- Les patients inclus dans des essais thérapeutiques et recevant un traitement anticancéreux oral dans ce cadre
- Les patients sous curatelle et tutelle